CBSE
 Multiple Choice Questions
Multiple Choice Questionsn = 2, l = 1
n = 3, l = 1
n = 3, l = 2
n = 3, l = o
16
8
36
18
n = 4, l = 0, ml = 0
n = 3, l = 2, ml = +1
n = 3, l = 0, ml = 0
n = 3, l = 1, ml = 1
m= 4, l = 0
n = 3, l = 1
n = 2, l = 1
n = 3, l = 2
2l + 1
2n2
4l + 2
2n2
n2
2l + 1
n
આપેલ પૈકી એક પણ નહી
10
30
25
5
18
23
24
16
12
36
72
6
n = 5, l = 2, ml = +1, s = 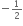
n = 4, l = 3, ml = -2, s = 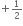
n = 6, l = 0, ml = 0, s = 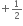
n = 5, l = 0, ml = 0, s =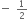
B.
n = 4, l = 3, ml = -2, s =