CBSE
 Multiple Choice Questions
Multiple Choice QuestionsMn2+ એ ઓટો ઉદ્દીપક તરીકે વર્તે છે.
નીપજ તરીકે CO2 ઉદ્દભવે છે.
પ્રક્રિયા ઉષ્માક્ષેપક છે.
MnO4- પ્રક્રિયાને ઉદ્દિપિત કરે છે.
મોહર ક્ષારના દ્રાવણનું KMnO4 વડે અનુમાપનમાં તેને જો 60°-70° તાપમાને ગરમ કરવામાં આવે, તો એક્યુરેટ પરિણામ આપે.
KMnO4 અને મોહર ક્ષાર વચ્ચેની પ્રક્રિયા ઠંડા દ્રાવણમાં શક્ય છે.
મોહર ક્ષારમાં હાજર ફેરસ સલ્ફેટને ગરમ ક્રવાથી તેનું હવા દ્વારા ફેરિક સલ્ફેટમાં ઍક્સિડેશન થાય છે.
PbCl2
Cu(NO3)2
BaCl2
CuCl2
C.
BaCl2
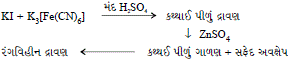
પ્રથમ પ્રક્રિયા એ રેડોક્ષ પ્રક્રિયા છે.
ગાળણમાં સ્ટાર્ચનું દ્રાવણ ઉમેરવાથી તે પીળો રંગ આપે છે.
સફેદ અવક્ષેપ એ Zn3[Fe(CN)6]2 ના છે.
સફેદ અવક્ષેપ એ NaOH ના દ્રાવણમાં દ્રાવ્ય છે.
 2H2O) નું 250 મિલિ જલીય દ્રાવણ બનાવવામં આવેલ છે. આ દ્રાવણના 10 મિલિનું સંપૂર્ણ તટસ્થીકરણ કરવા માટે 0.1 N NaOH ના દ્રાવણના કેટલા કદની જરૂર પડશે ?
2H2O) નું 250 મિલિ જલીય દ્રાવણ બનાવવામં આવેલ છે. આ દ્રાવણના 10 મિલિનું સંપૂર્ણ તટસ્થીકરણ કરવા માટે 0.1 N NaOH ના દ્રાવણના કેટલા કદની જરૂર પડશે ? 40 મિલિ
10 મિલિ
20 મિલિ
4 મિલિ
દ્રાવણને વધુ ગરમ કરવાને કારણે.
સતત ઠલાવતા રહીને ટીપે-ટીપે KMnO4 ઉમેરવાથી
મંદ H2SO4 ના ઓછા જથ્થાથી KMnO4 ના અપૂર્ણ રિડક્શનને લીધે.
હાઈડ્રોક્લોરિક ઍસિદ ઉમેરવાથી
HCl એ KMnO4 સાથે પ્રક્રિયા કરતો નથી.
KMnO4 એ HCl સાથે પ્રક્રિયા કરીને ક્લોરિન વાયુ ઉત્પન્ન કરે છે.
HCl સાથેની પ્રક્ર્યામં કેટલોક KMnO4 વપરાઈ જાય છે.
જેટલો જરૂર હોય તેના કરતા થોડો વધારે KMnO4 ની જરૂર પડે છે.
20 મિલિ
40 મિલિ
100 મિલિ
200 મિલિ
2.2 ગ્રામ
0.45 ગ્રામ
22.05 ગ્રામ
0.49 ગ્રામ
ટેટ્રાબોરેટ
આર્થોબેરોટ
મેટાબોરેટ
આપેલા ત્રણેય