CBSE
 Multiple Choice Questions
Multiple Choice Questions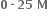 લેડનાઇટ્રેટ અને 25 મિલિ
લેડનાઇટ્રેટ અને 25 મિલિ  M ક્રોમિક સલ્ફેટનાં દ્વાવણોને મિશ્ર કરતાં લેડસલ્ફેટ અવક્ષેપિત થાય છે. કેટલા મોલ લેડસલ્ફેટ ઉત્પન્ન થશે ?પ્રક્રિયાને અંતે લેડનાઇટ્રેટની મોલારિટી કેટલી થશે ?
M ક્રોમિક સલ્ફેટનાં દ્વાવણોને મિશ્ર કરતાં લેડસલ્ફેટ અવક્ષેપિત થાય છે. કેટલા મોલ લેડસલ્ફેટ ઉત્પન્ન થશે ?પ્રક્રિયાને અંતે લેડનાઇટ્રેટની મોલારિટી કેટલી થશે ?



7.723, 3.865
3.865, 3.865
7.732, 7.732
3.865, 7.732
NO2 અને N2O4 ના મિશ્રણની બાષ્પઘનતા 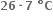 તાપમાને
તાપમાને  છે. 100 ગ્રામ મિશ્રણમાં NO2 ના મોલની સંખ્યા ગણો. (NO2 = 46, N2O4 = 92)
છે. 100 ગ્રામ મિશ્રણમાં NO2 ના મોલની સંખ્યા ગણો. (NO2 = 46, N2O4 = 92)
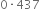
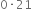

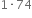
28
72
12
24
D.
24
સંયોજનનું સૂત્ર = M3 N2
તેથી સંયોજનમાં નાઈટ્રોજનની સંયોજકતા = 3 નાઈટ્રોજનનો તુલ્યભાર =
નાઈટ્રોજનનો તુલ્યભાર = 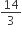
હવે, 28 ગ્રામ નાઈટ્રોજન 72 ગ્રામ ધાતુ સાથે સંયોજાય છે. 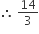 ગ્રામ નાઈટ્રોજન
ગ્રામ નાઈટ્રોજન 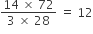 ગ્રામ ધાતુ સાથે સંયોજાય
ગ્રામ ધાતુ સાથે સંયોજાય ધાતુનો તુલ્યભાર = 12
ધાતુનો તુલ્યભાર = 12  ધાતુનો પરમાણુભાર= તુલ્યભાર
ધાતુનો પરમાણુભાર= તુલ્યભાર  સંયોજકતા
સંયોજકતા
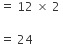
સંયોજનનું સૂત્ર = M3 N2
તેથી સંયોજનમાં નાઈટ્રોજનની સંયોજકતા = 3 નાઈટ્રોજનનો તુલ્યભાર =
નાઈટ્રોજનનો તુલ્યભાર = 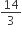
હવે, 28 ગ્રામ નાઈટ્રોજન 72 ગ્રામ ધાતુ સાથે સંયોજાય છે. 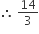 ગ્રામ નાઈટ્રોજન
ગ્રામ નાઈટ્રોજન 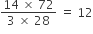 ગ્રામ ધાતુ સાથે સંયોજાય
ગ્રામ ધાતુ સાથે સંયોજાય ધાતુનો તુલ્યભાર = 12
ધાતુનો તુલ્યભાર = 12  ધાતુનો પરમાણુભાર= તુલ્યભાર
ધાતુનો પરમાણુભાર= તુલ્યભાર  સંયોજકતા
સંયોજકતા
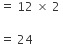
106 કિગ્રા
190 કિગ્રા
109 કિગ્રા
60 કિગ્રા

49
62
98
12
 3Fe(s) + 4CO2(g) પ્રક્રિયા દરમિયાન ઉત્પન્ન થતા લોખંડનું વજન ગણો.
3Fe(s) + 4CO2(g) પ્રક્રિયા દરમિયાન ઉત્પન્ન થતા લોખંડનું વજન ગણો.
1680 કિગ્રા
168 કિગ્રા
420 કિગ્રા
3360 કિગ્રા
જો  મોલ BaCl2 ને
મોલ BaCl2 ને  મોલ Na3PO4 સાથે મિશ્ર કરવામાં આવે Ba3(PO4)2 ના મહત્તમ કેટલા મોલ બનશે ?
મોલ Na3PO4 સાથે મિશ્ર કરવામાં આવે Ba3(PO4)2 ના મહત્તમ કેટલા મોલ બનશે ?




 ગ્રામ એક્ઝેલિકઍસિડડાયહાયડ્રેટનું 250 મિલિ જલીય દ્વાવણ બનાવવામાં આવ્યું. આ દ્વાવણના 10 મિલિ કદનું સંપૂર્ણ તટસ્થીકરણ કરવા
ગ્રામ એક્ઝેલિકઍસિડડાયહાયડ્રેટનું 250 મિલિ જલીય દ્વાવણ બનાવવામાં આવ્યું. આ દ્વાવણના 10 મિલિ કદનું સંપૂર્ણ તટસ્થીકરણ કરવા 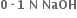 ના દ્વાવનનું કેટલું કદ જોઈશે ?
ના દ્વાવનનું કેટલું કદ જોઈશે ?20 મિલિ
4 મિલિ
10 મિલિ
40 મિલિ
 ગ્રામ કૉપર (II) કાર્બોનેટને ઓગાળવા કેટલા મિલિ
ગ્રામ કૉપર (II) કાર્બોનેટને ઓગાળવા કેટલા મિલિ  જોઇએ.
જોઇએ. 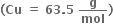
 મિલિ
મિલિ
 મિલિ
મિલિ
 મિલિ
મિલિ
 મિલિ
મિલિ