CBSE
 Multiple Choice Questions
Multiple Choice QuestionsRbF
KF
NaF
CsF
D.
CsF
CsF માં Cs+ નું કદ મોટું હોવાથી Cs+ અને F- વચ્ચેનું આકર્ષણ નિર્બળ હોવાથી CsF ની દ્વાવ્યતા વધુ હોય છે.
CsF માં Cs+ નું કદ મોટું હોવાથી Cs+ અને F- વચ્ચેનું આકર્ષણ નિર્બળ હોવાથી CsF ની દ્વાવ્યતા વધુ હોય છે.
LiBr
LiF
LiI
LiCl
મુક્ત ઇલેક્ટ્રૉન
મુક્ત અણુઓ
મુક્ત આયનો
Na અને Cl ના પરમાણુ
A ની આયનીકરણ એન્થાલ્પી ઓછી અને B ની ઇલેક્ટ્રોન પ્રાપ્તિ એન્થાલ્પી ઓછી
A ની આયનીકરણ એન્થાલ્પી વધુ અને B ની ઇલેક્ટ્રૉન પ્રાપ્તિ એન્થાલ્પી ઓછી
A ની આયનીકરણ એન્થાલ્પી ઓછી અને B ની ઇલેક્ટ્રૉન પ્રાપ્તિ એન્થાલ્પી વધુ
એકેયે નહી.
માત્ર આયનનો વીજભાર
આયનનો વીજભાર અને કદ
માત્ર આયનનું કદ
એકેય નહી
કદ નાનું
વીજભાર ઓછો
વીહભાર શૂન્ય
એકેય નહી
CsNO3
LiNO3
KNO3
NaNO3
વિધાન 1 અને 2 બંને સાચાં છે અને વિધાન 2 એ વિધાન 1 ની સમજૂતી આપે છે.
વિધાન 1 સાચું છે અને વિધાન 2 ખોટું છે.
વિધાન 1 અને 2 બંને સાચાં છે, પરંતુ વિધાન 2 એ વિધાન 1 ની સમજૂતી આપતું નથી.
વિધાન 1 ખોટું છે અને વિધાન 2 સાચું છે.
ચાર તત્વો L, Q, P અને R ની ઇલેક્ટ્રોન રચના નીચે મુજબ છે :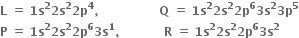
તો તેમના દ્વારા બનતા આયનીય સંયોજનોનાં સૂત્રો અનુક્રમે ............
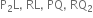
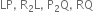
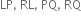
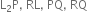
Al - Cl
C - Cl
Cs - Cl
H - Cl